
Modèlisation des molécules
_______________________
Auteur: Alain CHOYEAU, lycée Camille JULLIAN BORDEAUX
Pour illustrer les différentes manières de modèliser des molécules ,j'ai choisi une molécule simple de chimie organique , l'éthanol autrefois appelé alcool éthylique ou simplement alcool.
Ce corps , formé de deux atomes de carbone , de cinq atomes d'hydrogéne et d'un groupement fonctionnel alcool OH a pour formule brute C2H5OH .Il dérive de l'éthane , l'alcane à deux atomes de carbone ,en substituant le groupement fonctionnel de l'alcool OH à l'un quelconque des hydrogènes .Une première façon de progresser dans la description est de donner une formule développée dans notre page plane obéissant aux liaisons habituelles connues de chaque atome à savoir une liaison covalente pour un hydrogène , deux pour un oxygène et quatre pour un carbone .Ce qui nous conduit à la formule dite développée CH3CH2 (OH) .Cette écriture ne nous apprend rien sur les positions des atomes dans l'espace à trois dimensions ,aussi un dessin dans l'espace en tenant compte qu'aucun atome d' hydrogène de l'éthane occupe une position privilégiée nous amène à la première figure ci-dessous dite "en fil de fer".

Cette figure est dessinée avec les liaisons de différentes couleurs : blanches pour les H , grises pour les C , rouge pour l'oxygène .Le premier défaut qui apparaît est que deux liaisons peuvent être cachées par deux autres en avant-plan et que si nous voulons les voir ,il nous faut opérer une rotation autour d'un axe .De plus la masse des atomes n'est pas suggérée , nous ne devinons que les positions .En dessinant des bâtons ("sticks") à la place des traits nous obtenons un nouveau dessin un peu plus clair.

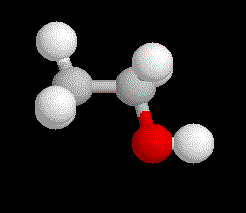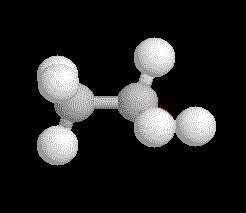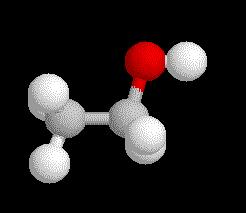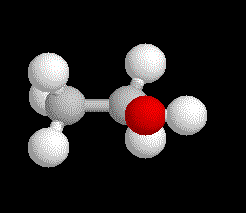
Puis en dessinant des sphères dont le diamètre suggère la grosseur des atomes correspondants ,nous obtenons le modèle qui sans doute se rapproche le plus de la réalité physique ,appelé modèle compact .

Ce modèle très satisfaisant nous cache pourtant les liaisons et les distances des atomes entre-eux .Aussi nous préfèrerons le modèle dit éclaté qui nous fournit les longueurs et direction des liaisons tout en donnant les grosseurs des atomes .

Pourquoi ne pas terminer par une animation faisant alors tourner la molécule autour d'un axe dans l'espace et vibrer les atomes ?
Si les images n'apparaissent pas , cliquez dessus avec le bouton gauche de la souris et rechargez les.
___________________________________________________________________________________________
© Administrateur Sciences-Physiques. Contact :
Alain.Choyeau@ac-bordeaux.fr© Rectorat de Bordeaux. Contact :
CATICE@ac-bordeaux.fr